近日,我所生物技术研究部生物分子高效分离与表征研究组(1810组)张丽华研究员、赵群研究员团队与精细化工研究室蛋白质折叠与聚集研究组(212组)刘宇研究员团队合作,开发出一种超光敏荧光蛋白仿生标签工具(upsFP tag),该工具可在相变蛋白质聚集后的紧实微环境中激活光催化反应活性,实现周围互作蛋白质的化学邻近标记,以及相分离蛋白质组组分变化规律的特异性解析。
随着人口老龄化问题日趋严峻,神经退行性疾病逐渐成为全球公共卫生领域的重大挑战。近年来,脊髓侧索硬化症(Amyotrophic Lateral Sclerosis,ALS,即“渐冻人症”)作为一种致命的神经退行性疾病,侵袭运动神经而导致肌肉无力与萎缩,引发社会广泛关注。尽管可通过肌电图、神经传导检测及影像学检查进行诊断,但渐冻人症的确切病因仍不明确,临床上对因治疗手段相对匮乏。病理研究结果表明,TDP43蛋白的相分离和相变聚集过程与渐冻人症的发生、发展机制密切相关。然而,原位捕获TDP43构象动态变化过程,以及解析活细胞内与其相互作用的蛋白质组仍具有挑战。
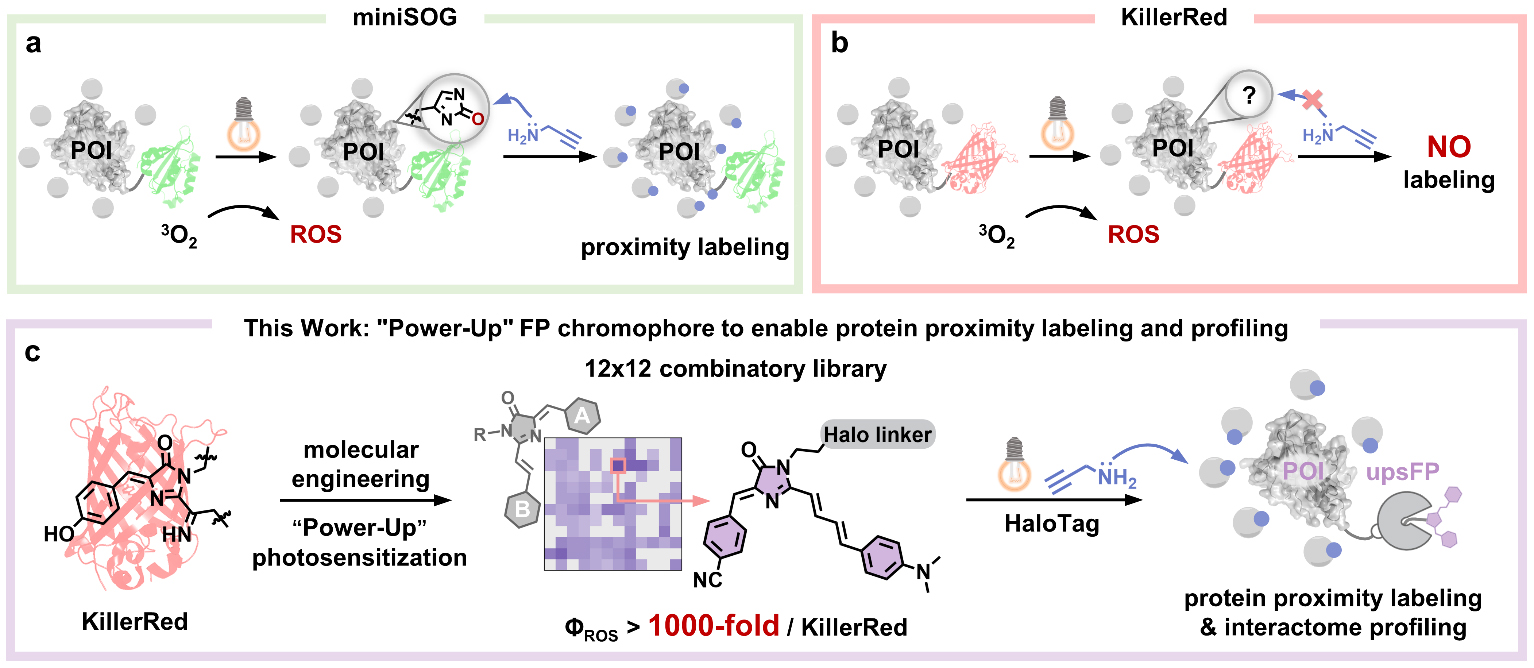
近年来,蛋白质空间邻近标记新技术的研制推动了蛋白质相互作用解析新技术的发展。然而,特异性捕获分离活细胞内相分离蛋白质组的鉴定方法鲜有报道。本工作中,研究团队以天然荧光蛋白的发色团为基础,通过调节探针的电子效应和重原子取代等化学策略,增强了发色团衍生物的三重态激发态光敏化性质,提升了其活性氧生成效率。与天然光敏荧光蛋白KillerRed方法相比,团队开发的最佳探针活性氧生成方法的效率提升超1000倍。进一步,团队利用串联质谱解析了该I型光敏剂标定蛋白质的分子机制,包括活性中间体、氨基酸标记位点和标记反应机理等。利用所构建的upsFP标签工具,研究团队通过蛋白质组学定量分析技术,鉴定了渐冻人症致病TDP43蛋白在细胞核内相分离之前、相分离之后,以及进一步固化迁移至细胞质形成蛋白质聚集体后的相互作用蛋白质组,解析了蛋白质伴随构象变化和亚细胞器穿梭过程互作组的动态变化规律。研究发现,细胞骨架蛋白高度参与了TDP43应激相变过程。
相关成果以“1000-fold Ultra-Photosensitized Fluorescent Protein Mimics towards Photocatalytic Proximity Labeling and Proteomic Profiling Functions”为题,发表在《先进科学》(Advanced Science)上,该工作的第一作者是我所212组博士研究生孙瑞。上述工作得到国家自然科学基金、我所创新基金等项目的资助。(文/图 孙瑞)
文章链接:https://doi.org/10.1002/advs.202413063