我所生物分离分析新材料与新技术研究组(1809组)叶明亮研究员团队发展了基于溶剂诱导蛋白质沉淀方法用于在蛋白质组水平探测药物靶标蛋白。在基于蛋白质组学技术平台的药物靶蛋白筛选方面,药物靶蛋白的系统鉴定在理解药物作用机制和毒副作用方面起着至关重要的作用。传统策略通常需要对小分子或药物进行修饰/衍生,这会改变小分子的特异性和/或亲和力,因此会导致鉴定的药物蛋白靶标呈现假阳性的结果。因此,迫切需要一种无需任何修饰即可探索药物与游离药物相互作用的方法。
近年来,已经开发了几种无需对药物或小分子进行修饰的方法来研究药物与蛋白质相互作用,如药物亲和力响应靶标稳定性测定(DARTS),基于氧化速率的蛋白质稳定性分析(SPROX),胞内热变化测分析(CETSA)和热蛋白质组分析(TPP)。这些方法的显著特征是不需要对药物进行修饰。引起蛋白变性和沉淀的方法,除了加热变性以外,还有很多,如有机溶剂沉淀、盐析沉淀等。以有机溶剂沉淀蛋白质为例,其沉淀的原因主要归因于两个因素,包括溶液的介电性质降低和蛋白质水合膜破坏导致的蛋白质溶解度降低。基于以上考虑,发展了基于溶剂沉淀筛选药物靶标蛋白方法,即溶剂诱导的蛋白沉淀(SIP)方法,用MTX和SNS-032两种模型药物评估了开发的SIP方法,并成功揭示了已知的靶标。SIP识别靶标结合的能力通过使用广谱激酶抑制剂星形孢菌素进一步验证,该抑制剂诱导了许多激酶靶标的稳定转移。同时,对格尔德霉素进行了系统研究,以发现潜在的蛋白质靶标。格尔德霉素脱靶的发现有助于了解格尔德霉素诱导的肝毒性模式的作用,并为HSP90抑制剂设计提供了信息。此外,SIP方法可以评估药物-靶标相互作用的亲和力,并确定了格尔丹霉素新靶标NDUFV1的Kd。我们期望将来在药物靶标发现和机理研究中广泛使用这种方法。
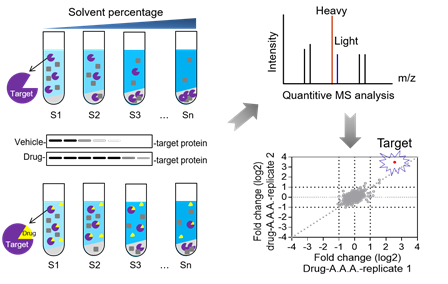
Anal. Chem.2020, 92, 1363−1371
相关成果发表在美国《分析化学》(Analytical Chemistry)等期刊上。该工作得到国家自然科学基金杰出青年基金、国家“万人计划”科技创新领军人才、辽宁省“兴辽英才”和大连化物所科研创新基金等项目资助。(文/图 刘晓艳)